Rôle dans nos métiers
Elle permet d’activer le dégagement gazeux de la levure chimique.
Elle est indispensable à la vitalité des diastases de la levure biologique.
Elle hydrate la farine, fait gonfler les particules d’amidon et assouplit le gluten.
Elle donne la plasticité nécessaire à la pâte pour retenir le dégagement de gaz carbonique lors de la fermentation (gonflement).
C’est le régulateur des glaces et sorbets.
Permet d’obtenir des solutions saturées ou sursaturées : pâtes de fruits, sirops, saumures…
C’est la première et plus utilisée des boissons.
C’est le principal agent nettoyant.
Eau potable
En France, l’eau est considérée comme potable si elle est conforme à la réglementation en vigueur, à savoir aux exigences des articles R1321.1 à R1321.5 du code de la santé publique et à celles des arrêtés d’application correspondants.
Une eau potable est définie au regard de toute une série de paramètres :
• des paramètres microbiologiques : bactéries, qui témoignent d’une contamination fécale (coliformes et streptocoques fécaux…)
• des paramètres chimiques : plomb, mercure, chlore, nitrates, pesticides…
• des indicateurs de radioactivité
• des paramètres organoleptiques : odeur, couleur, saveur.
Pour chacun des paramètres, des seuils sont imposés.
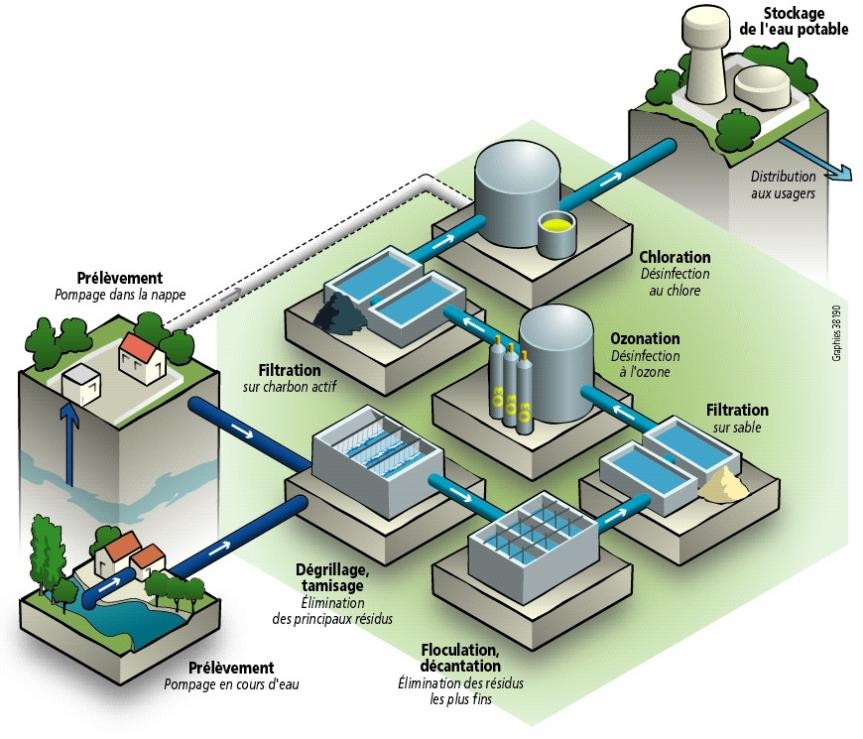
Les étapes de la production d'eau potable
Une fois prélevée, l'eau est soumise à plusieurs types de traitements :
• Dégrillage et tamisage. L'eau est d'abord filtrée à travers une grille afin d'arrêter les plus gros déchets, puis elle passe dans des tamis à mailles fines retenant des déchets plus petits.
• Floculation et décantation. Un coagulant est ajouté à l'eau pour rassembler en flocons les déchets encore présents (poussières, particules de terre, etc.). Ces flocons se déposent au fond du bassin de décantation ; 90 % des matières en suspension sont ainsi éliminées.
• Filtration. L'eau traverse un filtre, lit de sable fin et/ou un filtre à charbon actif. La filtration sur sable élimine les matières encore visibles à l'oeil nu. Les filtres à charbon actif retiennent les micro-polluants, comme les pesticides. Il existe des procédés de filtration encore plus poussés comme la filtration sur membranes.
• Ozonation. L'eau est désinfectée grâce à l'ozone, qui a une action bactéricide et antivirus. Ce gaz, mélangé à l'eau, agit aussi sur les matières organiques en les cassant en morceaux. Il améliore également la couleur et la saveur de l'eau.
• Chloration. Du chlore est ajouté à la sortie de l'usine de production et sur différents points du réseau de distribution afin d'éviter le développement de bactéries et de maintenir la qualité de l'eau tout au long de son parcours dans les canalisations.
L'eau
L’eau est un corps liquide, inodore et incolore. Elle est essentielle pour tous les organismes vivants connus. Elle recouvre 72 % de la surface de la Terre (97 % d’eau salée et 3 % d’eau douce dans différents réservoirs), mais l’eau est aussi présente sous forme gazeuse (vapeur d’eau) et solide (glace).
Composition et caractéristiques
L’eau dite « courante » est une solution d’eau contenant différents sels minéraux et gaz dissous contrairement à l’eau dite « pure » ou « distillée » utilisée en chimie. L’eau pure contient 2 atomes d’hydrogène et un atome d’oxygène, sa formule chimique est H2O.
Chaque eau possède une composition différente selon son origine et la nature du milieu qu’elle traverse : eau minérale, eau de source, eau de mer, eau douce, eau de pluie, eau gazeuse, eau plate…
PH de l’eau :
Pour connaitre l’acidité ou la basicité d’une eau on mesure son pH (potentiel hydrogène). L’échelle compte 14 graduations :
1 à 6 = pH acide ; entre 6 et 9 pH moyen ; de 9 à 14 = pH basique.
L’eau de boisson idéale aura un pH compris entre 6 et 7 selon le Professeur Louis-Claude VINCENT (1906-1988), ingénieur hydrologue français.
Dureté de l’eau :
Pour connaitre le degré de minéralisation d’une eau en sels calcium et sels magnésium on mesure sa dureté (titre hydrotimétrique : TH) exprimée en degré français (°F). Autrement dit, cet indicateur permet de connaitre le niveau de calcaire de l’eau (le calcaire n’est rien d’autre que du carbonate de calcium auquel s’ajoute du carbonate de magnésium). Plus l’eau en contient, plus elle sera « dure ».
L'eau est dite « douce » en dessous de 15 °F et « dure » au-delà de 25 °F.
L’eau douce a un pH inférieur à 7 et l’eau dure à un pH supérieur à 7.
Pour réduire la dureté de l'eau, on utilise un adoucisseur d'eau qui fonctionne grâce à une résine sur laquelle sont fixés des ions sodium. Les ions calcium et magnésium de l'eau dure sont échangés lors de leur passage sur la résine par des ions sodium.
Densité de l’eau :
La densité de l’eau est fixée à 1, c’est-à-dire que la masse d’un litre d’eau pèse 1 kg.
Phases de l’eau :
L’eau devient solide à 0°C, elle se transforme en glace.
L’eau est liquide entre 1 et 99°C.
L’eau s’évapore et devient un gaz à 100°C, une fois ce gaz refroidi on obtient de l’eau distillée (eau pure).
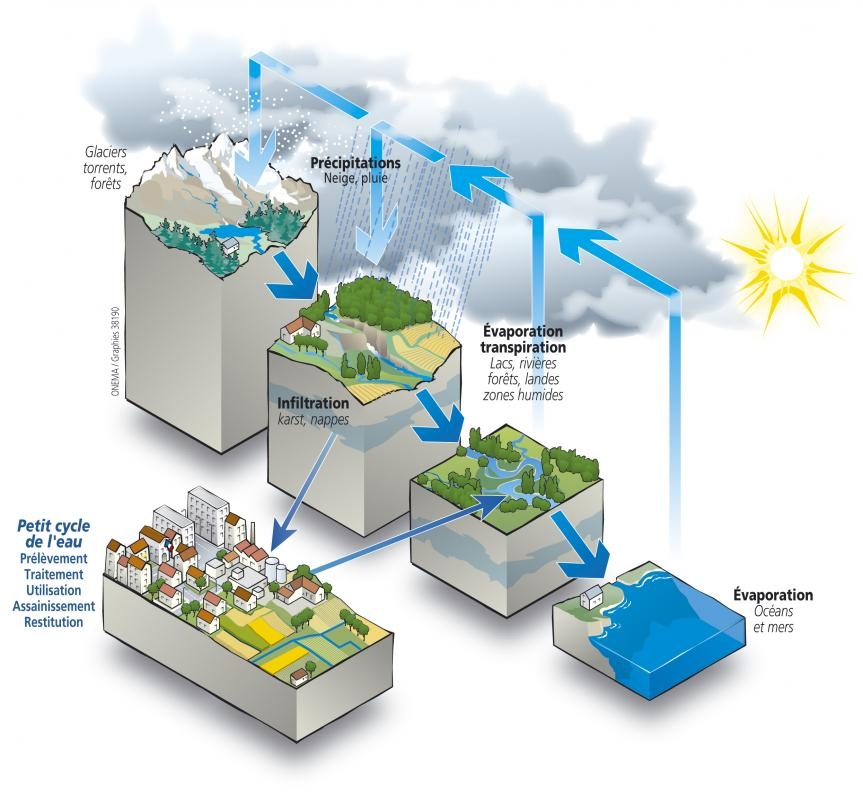
Cycle de l’eau
Sous l’action du soleil, une partie de l’eau de mer s’évapore pour former des nuages. Avec les vents, ces nuages arrivent au dessus des continents où ils s’ajoutent à ceux déjà formés. Lorsqu’il pleut, qu’il neige ou qu’il grêle sur ces mêmes continents, une partie de l’eau de ces précipitations repart plus ou moins rapidement dans l’atmosphère soit en s’évaporant directement, soit du fait de la transpiration des végétaux et des animaux. Une deuxième partie, en ruisselant sur le sol, rejoint assez vite les rivières et les fleuves puis la mer. Quant au reste, il s’infiltre dans le sol et est stocké en partie dans des nappes. Cette eau finira aussi par retourner à la mer, à beaucoup plus longue voire très longue échéance, par le biais des cours d’eau que ces nappes alimentent. Par ailleurs, sous l’action du soleil, de l’eau de mer continue de s’évaporer…
C‘est ce mouvement perpétuel de l’eau, sous tous ses états, qu’on appelle le grand cycle de l’eau.




















Copyright © 2009-2021 Patisland, tous droits réservés. Patisland ® et le logo sont des marques protégés.